肽
此條目可参照英語維基百科相應條目来扩充。 (2021年1月1日) |

綠色 標示 氨基端 (L-纈氨酸)
藍色 標示 羧基端 (L-丙氨酸).
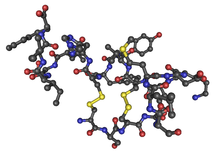


肽是天然存在的生物小分子,屬介於胺基酸和蛋白質之間的物質。其英語 peptide 源自古希臘語 πέπτω(péptō),義為“軟化、使熟、消化”[9]。由於胺基酸的分子最小,蛋白質最大,而肽則是氨基酸單體組成的短鏈,由肽(酰胺)鍵連接。當一個氨基酸的羧基基團與另一個氨基酸的氨基反應時,形成該共價化學鍵。
二胜肽(又稱二肽),就是由二個胺基酸組成的蛋白質片段,兩個或以上的胺基酸脫水縮合形成若干個肽鍵從而組成一個肽,多個肽進行多級折叠就組成一個蛋白質分子。一般將 2-20肽歸於寡肽,20-50肽歸於多肽,通常十肽以下者較具醫藥及商業實用性。
水解法
[编辑]肽可由膳食蛋白質(dietary protein)通過化學方法水解出來,也可以人工方法取得。係由兩個或以上的胺基酸聚合所構成,在細胞生理及代謝功能的調節上甚為重要。肽大多性质不稳定,长期贮存宜防潮,放在4°C以下的地方。
用途
[编辑]活性肽與營養、荷爾蒙、酵素抑制、調節免疫、抗菌、抗病毒[10]、抗氧化有非常緊密關係。

結構
[编辑]肽是由氨基酸的胺基(-NH2)和羧基(-COOH)脱水缩合形成肽键後,形成的鏈狀分子。
肽鍵是由一個胺基酸與次一胺基酸的胺基,行脫水縮合反應而成的-CO-NH-鍵,具有雙鍵的性質,與鄰近共六個原子在同一平面上,因此C-N不可自由轉動,肽鍵是構成蛋白質架構的連繫帶。
对于含半胱氨酸,甲硫氨酸或色氨酸的肽,脱氧缓冲剂对其溶解必不可少,这类肽易于空气中氧化。含谷氨酰胺或天冬酰胺的多肽也容易降解。多肽在-20℃很稳定,特别是冷冻干燥并保存在干燥器中,在将它们暴露于空气之前,冷冻干燥多肽可以放于室温。
腖
[编辑]參考資料
[编辑]- ^ 审定公布名词数据库:31 条. 全国科学技术名词审定委员会. [2023-12-22]. (原始内容存档于2023-12-22) –通过术语在线.
- ^ 肽 peptide. 樂詞網.
- ^ 胜肽 peptide. 樂詞網.
- ^ 肽;縮胺酸類 peptide. 樂詞網.
- ^ Hamley, I. W. introduction to Peptide Science. Wiley. September 2020 [2023-12-22]. ISBN 978-1-119-69817-3. (原始内容存档于2021-03-09).
- ^ Nelson, David L.; Cox, Michael M. (2005). Principles of Biochemistry (4th ed.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ^ Saladin, K. Anatomy & physiology: the unity of form and function 6th. McGraw-Hill. 13 January 2011: 67. ISBN 978-0-07-337825-1.
- ^ 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "proteins"。doi:10.1351/goldbook.P04898.
- ^ 存档副本. [2023-12-22]. (原始内容存档于2023-12-22).
- ^ 科學人-分秒不鬆懈的人體免疫防禦系統

