1,2-苯二硫酚
外观
| 1,2-苯二硫酚 | |
|---|---|
| |

| |
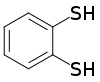
| IUPAC名 Benzene-1,2-dithiol | |
| 识别 | |
| CAS号 | 17534-15-5 |
| PubChem | 69370 |
| ChemSpider | 13840080 |
| SMILES |
|
| InChI |
|
| InChIKey | JRNVQLOKVMWBFR-UHFFFAOYAM |
| 性质 | |
| 化学式 | C6H6S2 |
| 摩尔质量 | 142.24 g·mol−1 |
| 外观 | 无色液体 |
| 密度 | 1.236 g/mL |
| 熔点 | 22—24 °C(72—75 °F;295—297 K) |
| 沸点 | 119—120 °C(246—248 °F;392—393 K)(17 mmHg) |
| 溶解性(水) | 可溶于碱性水溶液 |
| 危险性 | |
| 主要危害 | 恶臭 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
1,2-苯二硫酚是有机硫化合物,化学式为C6H4(SH)2。该化合物是无色粘稠液体,一个分子含有一个苯环和两个相邻的硫醇基。这个二元化合物的共轭碱用作配位化学的螯合剂,和其他有机硫化合物的合成砌块。[1]
合成
[编辑]用正丁基锂将苯硫酚邻位锂化,再加以硫化,便可制备这个化合物:[2]
- C6H5SH + 2 BuLi → C6H4SLi-2-Li + 2 BuH
- C6H4SLi-2-Li + S → C6H4(SLi)2
- C6H4(SLi)2 + 2 HCl → C6H4(SH)2 + 2 LiCl
该化合物最初由2-氨基苯硫醇的重氮化制备。[3]它也可以从1,2-二溴苯制备。[4]
反应
[编辑]1,2-苯二硫酚被氧化后会生成聚合物二硫化物;与金属二卤化物和金属氧化物反应时,会生成二硫醇盐配合物,化学式为LnM(S2C6H4),其中LnM代表各种金属中心,例如(C5H5)2Ti;会与酮和醛发生缩合反应,生成二硫杂环己烷:
- C6H4(SH)2 + RR'CO → C6H4(S)2CRR' + H2O
有关化合物
[编辑]3,4-甲苯二硫酚的行为与1,2-苯二硫酚的相似,但在室温下是固体(熔点:135-137 °C)。
1,2-烯二硫醇不稳定,但已知有1,2-烯二硫醇盐的金属配合物,称为二硫烯醇复合物。[1]
参考文献
[编辑]- ^ 1.0 1.1 Karlin, K. D.; Stiefel, E. I., Eds. “Progress in Inorganic Chemistry, Dithiolene Chemistry: Synthesis, Properties, and Applications” Wiley-Interscience: New York, 2003. ISBN 0-471-37829-1
- ^ D. M. Giolando; K. Kirschbaum. An efficient one-pot synthesis of 1,2-benzenedithiol from benzenethiol. Synthesis. 1992, 1992 (5): 451–452. doi:10.1055/s-1992-26132.
- ^ P. C. Guha; M. N. Chakladar. Dithiocatechol. J. Indian Chem. Soc. 1925, 2: 318.
- ^ Aldo Ferretti. "1,2-Dimercaptobenzene". Org. Synth.; Coll. Vol. 5: 419.
