氟化鋇
外觀
| 氟化鋇 | |
|---|---|

| |
| |
| 英文名 | Barium fluoride |
| 識別 | |
| CAS號 | 7787-32-8 |
| PubChem | 62670 |
| ChemSpider | 56421 |
| SMILES |
|
| InChI |
|
| InChIKey | OYLGJCQECKOTOL-NUQVWONBAV |
| RTECS | CQ9100000 |
| 性質 | |
| 化學式 | BaF2 |
| 摩爾質量 | 175.34 g·mol⁻¹ |
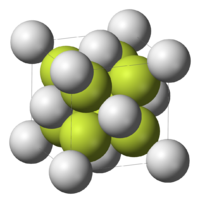
| 外觀 | 白色立方結晶 |
| 密度 | 4.893 g/cm3 |
| 熔點 | 1368 °C |
| 沸點 | 2260 °C |
| 溶解性(水) | 0.16 g/100 mL (20 °C) |
| 溶解性 | 可溶於甲醇、乙醇 |
| 結構 | |
| 晶體結構 | 螢石型結構,cF12 |
| 空間群 | Fm3m, No. 225 |
| 危險性 | |
| 歐盟危險性符號 | |
| 警示術語 | R:R20/22 |
| 安全術語 | S:S2, S28 |
| 歐盟編號 | 056-002-00-7 |
| NFPA 704 | |
| 致死量或濃度: | |
LD50(中位劑量)
|
250 mg/kg (大鼠經口) |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
性質
[編輯]在自然界中以氟鋇礦(frankdicksonite)的形式存在。[1]
結構
[編輯]固態氟化鋇為螢石型晶體結構,立方晶系。高壓下轉變為氯化鉛型結構。[2]
氣態時,以 BaF2 分子的形式存在,F-Ba-F 鍵角約為 108°,與價層電子對互斥理論的預測相矛盾。[3] 從頭計算的結果顯示這是鋇原子的 d 軌道參與的結果。[4] 也有理論認為這是由鋇內層電子的極化作用,在鋇原子周圍產生四面體型的電荷分布,並與 Ba-F 鍵發生作用造成的。[5]
製取
[編輯]一般由碳酸鋇與水調成的漿液與氫氟酸進行反應,再經過濾、乾燥、粉碎得到成品。
用途
[編輯]用於光學玻璃、電機電刷、光導纖維、激光發生器、塗料、助熔劑及琺瑯。用作木材防腐劑和殺蟲劑。[6]
參見
[編輯]閃爍體致光物質
參考資料
[編輯]- ^ Radtke A.S., Brown G.E. Frankdicksonite, BaF2, a New Mineral from Nevada. American Mineralogist. 1974, 59: 885-888.
- ^ A.F Wells. Structural inorganic chemistry -5th Edition. Oxford: Clarendon Press. 1984. ISBN 0-19-855370-6.
- ^ Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Seijo, Luis. Ab initio model potential study of the equilibrium geometry of alkaline earth dihalides: MX2 (M=Mg, Ca, Sr, Ba; X=F, Cl, Br, I). The Journal of Chemical Physics. 1991, 94: 3762. doi:10.1063/1.459748.
- ^ Bytheway, Ian. Core Distortions and Geometries of the Difluorides and Dihydrides of Ca, Sr, and Ba. Inorganic Chemistry. 1995, 34: 2407. doi:10.1021/ic00113a023.
- ^ 化學工業出版社組織編寫. 中国化工产品大全 上卷. 北京: 化學工業出版社. 1994年7月: 39. ISBN 7-5025-1268-3.


