蜀黍氰苷
| 蜀黍氰苷 | |
|---|---|
| |
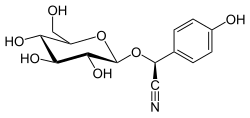
| IUPAC名 (S)-(β-D-Glucopyranosyloxy)(4-hydroxyphenyl)acetonitrile | |
| 系统名 (S)-(4-Hydroxyphenyl){[(2R,3R,4S,5S,6R)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy}acetonitrile | |
| 别名 | 蜀黍苷,对羟基苯甲醛氰醇葡萄糖苷 |
| 识别 | |
| CAS号 | 499-20-7 |
| PubChem | 161355 |
| ChemSpider | 141737 |
| SMILES |
|
| InChI |
|
| InChIKey | NVLTYOJHPBMILU-YOVYLDAJBT |
| 性质 | |
| 化学式 | C14H17NO7 |
| 摩尔质量 | 311.29 g·mol⁻¹ |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
蜀黍氰苷(英语:Dhurrin),简称蜀黍苷,学名对羟基苯甲醛氰醇葡萄糖苷,是一种存在于许多植物,特别是高粱(别名蜀黍)中的生氰糖苷,可在动物体内分解出有毒的氢氰酸(HCN)引起人畜氢氰酸中毒[1][2][3]。1906年曾发生过大规模牛氢氰酸中毒事件,并导致人们在许多高粱品种中发现了这一物质[4]。因其常见于高粱植株中,世界各地都有牲畜因误食高粱植株引起的中毒报告[5][6]。
生物合成与分布
[编辑]高粱中的产生途径以及分布
[编辑]在高粱中,蜀黍氰苷由酪氨酸转化得到,其产生受转录水平、生长年龄以及含有的营养物质影响。酪氨酸到蜀黍氰苷的转化过程涉及三种酶,CYP79A1酶和CYP71E1酶两种细胞色素P450酶,以及一个UDP-糖基转移酶UGT85B1。CYP79A1酶首先将酪氨酸进行两步连续的N-羟基化,随后脱水和脱羧得到对羟基苯基乙醛肟。对羟基苯基乙醛肟通过CYP71E1酶转化成对羟基扁桃腈,最后在水溶性的UDP-糖基转移酶作用下糖基化形成蜀黍氰苷[7][1]。

由于前两种酶为膜锚定的细胞P450酶,因此酪氨酸到对羟基扁桃腈过程发生在内质网的胞质表面。由于苯环上的酚羟基在碱性条件下不稳定,因此合成的蜀黍氰苷储存在酸性液泡中[1]。
蜀黍氰苷的合成很大程度上受CYP79A1和CYP71E1两种酶表达的影响。两种酶基因的转录和翻译在生长初期几日内最活跃,并在一周后大幅下降,并于5周后在叶片中低于测出水平[7],因此蜀黍苷在高粱不同部位中浓度不同,在种子中很低甚至没有,且在发芽前后几乎不受影响。在发芽后,地上部分、根部以及整株幼苗蜀黍苷含量明显增加。总体上,蜀黍氰苷在地上部分比地下部分高;叶片比茎高,尤其幼苗的第一片叶子最高[1]。
转基因合成
[编辑]研究表明,将CYP79A1和CYP71E1植入到拟南芥和烟草基因组中可使得两种植物产生蜀黍氰苷[8]。 这两种酶对于蜀黍氰苷的产生都是充分且必要的,因为从高粱基因组中敲去CYP79A1基因后,高粱不再产生蜀黍氰苷。发生干旱时,高粱往往是唯一可用的谷物,因此在理论上敲除这种基因的高粱可以作为干旱条件下更安全的饲料。在体外实验中,人们已经在从高粱幼苗中提取的微粒体和胶束中实现了的蜀黍氰苷的体外合成[9]。
毒性
[编辑]哺乳动物毒性
[编辑]蜀黍氰苷本身无毒性,但摄入哺乳动物体内后受肠道中的β-葡萄糖苷酶作用水解糖苷键形成葡萄糖和苷元对羟基扁桃腈,对羟基扁桃腈受α-羟腈酶作用迅速降解形成氢氰酸和对羟基苯甲醛[3],氢氰酸与细胞色素C氧化酶中Fe3+离子结合阻断呼吸链,引起细胞中毒性缺氧,产生相应的中毒症状[1]。理论上蜀黍氰苷对人和其他哺乳动物的致死量很高,因为一分子蜀黍氰苷只产生一个氢氰酸,而高粱植株中蜀黍氰苷含量较低,比如一般酿酒用的高粱品种含量为4.52-19.28 mg/kg[2],因此人类需食用大量的生高粱才会出现不良反应[10]。
由于发生干旱时高粱是最佳的可用的谷物或饲料,加之高粱在干旱和酷热下容易产生蜀黍氰苷[11],因此干旱期间往往是牲畜蜀黍氰苷中毒高发期[10]。比如2022年夏季干旱期间,意大利皮埃蒙特多个农场发生牛食用高粱导致的中毒事件,共造成50头牛死亡[6][12]。据记录,牛误食高粱植株后中毒症状会出现倒地不起、口吐白沫、呼吸困难、肌肉震颤等症状,严重的可引起死亡[5][6]。
昆虫毒性
[编辑]蜀黍氰苷和其他生氰糖苷一样,是植物的防御物质。当不同高粱品种的茎受到外部损伤时,在损伤部位释放出蜀黍氰苷。这种反应已被证明可以驱赶昆虫,因为与野生型品种相比,经转基因改造不能产生蜀黍氰苷的高粱更容易受食草昆虫青睐[13]。
高粱酿酒中有害物质
[编辑]在白酒酿造过程中,蜀黍氰苷可经β-葡萄糖苷酶等酶分解产生氢氰酸,亦或者受热分解产生氰醇,氰醇进一步分解形成氢氰酸。氢氰酸经Cu2+的催化下生成氰酸盐,氰酸盐沸点较低,极容易在蒸酒过程中蒸发出来进入酒体,最终与酒精反应生成具有遗传毒性和致癌性的氨基甲酸乙酯[14][3][2]。
参考文献
[编辑]- ^ 1.0 1.1 1.2 1.3 1.4 吴荣,牛江帅,岩温香,等. 高粱蜀黍苷的研究进展. 中国粮油学报. 2021, 36 (12): 172–178. doi:10.3969/j.issn.1003-0174.2021.12.026.
- ^ 2.0 2.1 2.2 周韩玲,安明哲,赵东,等. 不同产地及品种高粱中蜀黍氰苷含量的差异化分析. 中国酿造. 2023, 42 (7): 209–213. doi:10.11882/j.issn.0254-5071.2023.07.034.
- ^ 3.0 3.1 3.2 周韩玲,安明哲,赵东,等. 高粱中蜀黍氰苷与浓香型白酒中氰化物及氨基甲酸乙酯关系的研究. 中国酿造. 2022, 41 (10): 25–29. doi:10.11882/j.issn.0254-5071.2022.10.005.
- ^ Blyth, Alexander Wynter. Poisons: Their Effects and Detection A Manual for the Use of Analytical Chemists and Experts. USA: Charles Griffin and Company. May 13, 2013: 204.
- ^ 5.0 5.1 黄纯武. 高粱嫩苗导致水牛氢氰酸中毒的病例报告. 广西畜牧兽医. 2007, 23 (4): 182-183. doi:10.3969/j.issn.1002-5235.2007.04.022.
- ^ 6.0 6.1 6.2 Stefano Giantin,Alberico Franzin,Giovanni Topi,; et al. Outbreaks of lethal cyanogenic glycosides poisonings of cattle after ingestion of Sorghum ssp. grown under drought conditions in August 2022 in Piedmont (North-Western Italy). Large Animal Reviews. 2023, 29 (4).
- ^ 7.0 7.1 7.2 Busk, Peter Kamp. Dhurrin Synthesis in Sorghum Is Regulated at the Transcriptional Level and Induced by Nitrogen Fertilization in Older Plants. Plant Physiology. July 2002, 129 (3): 1222–1231. PMC 166516
 . PMID 12114576. doi:10.1104/pp.000687.
. PMID 12114576. doi:10.1104/pp.000687.
- ^ Bak, Soren. Transgenic Tobacco and Arabidopsis Plants Expressing the Two Multifunctional Sorghum Cytochrome P450 Enzymes, CYP79A1 and CYP71E1, Are Cyanogenic and Accumulate Metabolites Derived from Intermediates in Dhurrin Biosynthesis. Plant Physiology. August 2000, 123 (4): 1437–1448. PMC 59100
 . PMID 10938360. doi:10.1104/pp.123.4.1437.
. PMID 10938360. doi:10.1104/pp.123.4.1437.
- ^ Kahn, R A. Isolation and reconstitution of cytochrome P450ox and in vitro reconstitution of the entire biosynthetic pathway of the cyanogenic glucoside dhurrin from sorghum.. Plant Physiology. December 1997, 115 (4): 1661–1670. PMC 158632
 . PMID 9414567. doi:10.1104/pp.115.4.1661.
. PMID 9414567. doi:10.1104/pp.115.4.1661.
- ^ 10.0 10.1 Borrell, Andrew K. Drought adaptation of stay-green sorghum is associated with canopy development, leaf anatomy, root growth, and water uptake. Journal of Experimental Botany. 2014, 65 (21): 6251–6263. PMC 4223986
 . PMID 25381433. doi:10.1093/jxb/eru232.
. PMID 25381433. doi:10.1093/jxb/eru232.
- ^ Cyanide (prussic acid) and nitrate in sorghum crops - managing the risks. Primary industries and fisheries. Queensland Government. 存档副本. [2015-09-08]. (原始内容存档于2012-03-19).. 21 April 2011.
- ^ Redazione ANSA. 50 grazing cows fatally poisoned by sorghum.
- ^ Krothapalli, Kartikeya. Forward Genetics by Genome Sequencing Reveals That Rapid Cyanide Release Deters Insect Herbivory of Sorghum Bicolor (PDF). Genetics. October 2013, 195 (2): 309–318. PMC 3781961
 . PMID 23893483. doi:10.1534/genetics.113.149567.
. PMID 23893483. doi:10.1534/genetics.113.149567.
- ^ Michele Aresta,Maurício BoscoloDouglas,Wagner Franco. Copper(II) Catalysis in Cyanide Conversion into Ethyl Carbamate in Spirits and Relevant Reactions. Journal of Agricultural and Food Chemistry. 2001, 49 (6): 2819–2824. doi:10.1021/jf001346w.
